CASO CLÍNICO
Antecedentes
Mujer de 37 años. Sin alergias medicamentosas conocidas. Antecedente personal de neoplasia de mama avanzada con progresión ósea (esternal, costal, parietal y occipital), hepática y pulmonar; en cuarta línea de tratamiento quimioterápico y en cuidados paliativos.
Enfermedad actual
Progresión adenopática supraclavicular y retropectoral izquierda en forma de un conglomerado de 6,5 x 3,9 cm que origina un dolor neuropático grave en extremidad superior izquierda debido a la compresión del plexo braquial. Impacto funcional y emocional negativo. El dolor es constante tanto en reposo como en movimiento, se asocia a incapacidad para movilizar objetos ligeros e interrumpe el sueño nocturno. Mal control del mismo a pesar de tratamiento intensivo con opiáceos mayores vía oral y subcutánea y neuromoduladores vía oral. Se realiza el cuestionario de la escala visual analógica (EVA) siendo esta 10/10 previa a la técnica.
Exploración física
Regular estado general. Masa supraclavicular destechada sin signos de infección. Dolor de características neuropáticas en extremidad superior izquierda con alodinia y parestesias en todo el territorio inervado por el plexo braquial.
Exploraciones complementarias
Se realiza TAC torácico donde se observa una masa tumoral esternal con extensión a pared torácica anterior y al mediastino.
Se objetiva progresión adenopática en forma de conglomerados izquierdos a nivel supraclavicular de 6.5 x 3.4 cm y otro subyacente clavicular/retropectoral de 6 x 4cm (medidos en plano coronal). Estos provocan estenosis del tronco venoso braquicefálico izquierdo y venas subclavia y yugular izquierdas. Imagen sugestiva de trombo en vena subclavia izquierda.
Además, presenta metástasis óseas en arco posterior de quinta costilla derecha con abundante componente intratorácico (69 mm), arco posterior de sexta costilla derecha (13 mm), octava costilla izquierda y vértebra D5.
Diagnóstico
Dolor neuropático en el territorio del plexo braquial izquierdo a causa de compresión por metástasis adenopática supraclavicular.
Diagnóstico diferencial
Por los antecedentes de neoplasia avanzada, las pruebas de imagen y los resultados de anatomía patológica se puede descartar que se trate de linfadenopatía reactiva/infecciosa como infecciones virales (EBV, CMV, VIH), bacterianas (tuberculosis, toxoplasmosis, bartonella, Kikuchi.Fujimoto) y hongos o micobacterianas atípicas. También, neoplasias hematológicas como linfomas, una anomalía congénita u otro tumor primario de novo (ya sea in situ de tejidos blandos del cuello o bien adenopatía metastática).
Tratamiento
Debido a la mala respuesta al tratamiento con opioides mayores a dosis altas y neuromoduladores se decide colocación de catéter interescalénico bajo visión ecográfica con equipo de aguja estimulable y comprobación con neuroestimulación.
Se coloca a la paciente en decúbito supino con la cabeza girada hacia el lado opuesto al que se bloquea y se realiza asepsia de la zona. A continuación, se moviliza lentamente el transductor en dirección cefálica mientras se visualiza de forma continua el plexo braquial hasta identificarlo entre los músculos escalenos anterior y medio (Fig. 1). Debido a la presencia de una masa adenopática estos se encuentran desplazados cranealmente y presentan una leve distorsión anatómica. Mediante un abordaje en plano y con el uso de neuroestimulación, se introduce la aguja de lateral a medial, localizando el plexo a 2 cm de profundidad y se procede a la colocación del catéter. Tras una aspiración cuidadosa se administran 8 ml de lidocaína 2%, con reducción significativa del dolor (EVA 5-6/10). Posteriormente, se mantiene una infusión continua a 2 ml/h de ropivacaína 2% + fentanilo (2 mcg/ml).
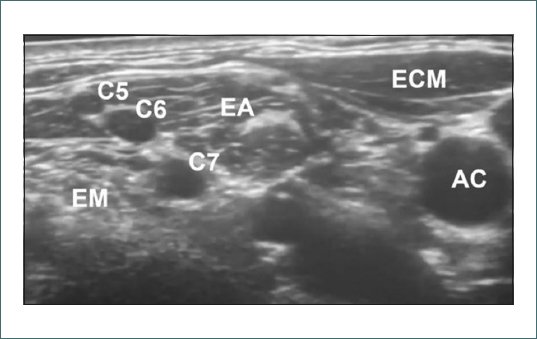
Figura 1. Ultrasonido del plexo braquial a nivel interescalénico. C5, C6, C7: nervios espinales cervicales del quinto al séptimo; EM: escaleno medio; EA: escaleno anterior; ECM: esternocleidomastoideo; AC: arteria carótida.
Paralelamente se instaura perfusión endovenosa continua de ketamina a 0,1mg/kg/h bajo supervisión de enfermería de planta de oncología.
Evolución
Tras el procedimiento, se realiza un seguimiento diario de la paciente para evaluar su evolución. La estrategia implementada permite un control óptimo del dolor, evidenciándose una disminución del 80% en la escala EVA (de 10/10 a 2/10 a las 24 horas de iniciado el tratamiento), junto con una mejoría significativa en la limitación funcional y en la percepción de bienestar.
Esta mejoría facilita la reducción de opioides mayores, siendo necesarios únicamente rescates puntuales con metadona subcutánea. La evolución clínica se mantiene favorable en los días posteriores.
De forma paralela, y ante la progresión de la enfermedad, se instauran medidas de confort y sedación paliativa.
DISCUSIÓN
El cáncer es la segunda causa de mortalidad en nuestro país y el dolor es el síntoma más común que acompaña a casi todos los pacientes hasta el final de sus vidas. Se calcula que la prevalencia del dolor relacionado con el cáncer oscila entre el 30 y el 50% en los pacientes en tratamiento crónico. El 33% de los pacientes que reciben tratamiento activo del cáncer con metástasis padecen un dolor significativo relacionado con el propio tumor, y este porcentaje aumenta hasta el 60-90% en los que presentan cáncer avanzado1.
Según el origen y las características, el dolor puede ser de varios tipos: nociceptivo (somático o visceral), neuropático o psicógeno. Un elevado porcentaje de los pacientes (40-60%) presentan dolor neuropático o mixto, lo que complica significativamente su abordaje terapéutico y contribuye a una mayor limitación funcional1.
El dolor neuropático es el dolor causado o iniciado por una lesión o enfermedad del sistema nervioso, ya sea central o periférico y puede ser de características lancinantes o presentarse de forma crónica. Se acompaña de alteraciones sensitivas, disestesia, parestesias, alodinia e hiperalgesia. Los cuadros clínicos más frecuentes en pacientes oncológicos son: plexopatía lumbosacra o braquial (infiltración tumoral, radioterapia), neuropatía periférica (plexitis postradioterapia, polineuropatía por platino) o compresión medular1.
Se estima que hasta un 31% de los pacientes con dolor oncológico no reciben el tratamiento adecuado y hasta un 10-20% pueden presentar dolor refractario, dolor que no responde al tratamiento estándar con opioides y terapia adyuvante. Este tipo de dolor debe tratarse de forma multidisciplinar desde las Unidades de Dolor, que abarca desde técnicas intervencionistas tanto a nivel de nervios periféricos (bloqueos, radiofrecuencia, ablación, neuroestimulación) como a nivel central (neuroestimulación, analgesia epidural o intradural) y el uso de coadyuvantes farmacológicos asociados a estas1.
El bloqueo interescalénico es una técnica locorregional que aborda el plexo braquial en su parte más proximal. El plexo braquial se forma por las comunicaciones que se establecen entre los ramos anteriores de los nervios espinales de C5 a T1 (en 2/3 de los pacientes también de C4 y en 1/3 de los pacientes también de T2), siendo muy frecuentes las variaciones anatómicas interpersonales. Estos ramos anteriores pasan por detrás de la arteria vertebral y se dirigen horizontal y lateralmente por la superficie superior de las apófisis transversas. Luego, convergen formando tres troncos (C5-C6, C7, C8-T1) situados entre los escalenos anterior y medio (espacio interescalénico) y se dirigen de forma descendente y lateral hacia el hueco axilar2.
Proporciona inervación sensitiva y motora para todo el miembro superior, excepto una zona adyacente al hombro, cuya sensibilidad depende de los nervios supraclaviculares (plexo cervical), y la parte interna del brazo que depende de los nervios intercostobraquiales (ramos del segundo y tercer nervios intercostales)3.
Se trata de un bloqueo con una tasa de éxito muy alta y una baja incidencia de eventos adversos. Aunque la guía ecográfica ha incrementado considerablemente la seguridad del procedimiento, persisten ciertos riesgos inherentes a la técnica4.
Entre las posibles complicaciones específicas de este abordaje se incluyen: neumotórax, por su proximidad a la pleura; difusión del anestésico local a estructuras vecinas, lo que puede provocar disfonía y ronquera (por parálisis transitoria del nervio laríngeo recurrente), parálisis hemidiafragmática (por afectación del nervio frénico) o síndrome de Horner (por bloqueo del ganglio cervical). También pueden presentarse inyecciones epidurales o intradurales, inyección vascular, lesión del plexo braquial, neuropatía o infección5.
En casos de dolor localizado, las técnicas locorregionales ofrecen una alternativa válida y más aconsejable que la vía sistémica al evitar la aparición de efectos secundarios y mejorar la calidad de la analgesia, sobre todo en pacientes oncológicos con dolor refractario a dosis altas de opioides y adyuvantes6.
En relación a los fármacos coadyuvantes tiene especial interés la ketamina.
La ketamina es un derivado de la phencyclidina, sintetizada en 1962. Sus efectos psicodélicos hicieron que quedara rápidamente limitada a su uso en animales. En el 1984 fue añadida a la lista de medicamentos esenciales de la Organización Mundial de la Salud como anestésico endovenoso, pero a partir de 1990, con el descubrimiento de nuevos hipnóticos como el propofol, se limitó su uso en desastres naturales, guerras y tercer mundo. Con la llegada del nuevo siglo y el aumento del conocimiento sobre su farmacocinética y su mecanismo de acción han producido un renacimiento de la misma. En la actualidad su uso se ha extendido más allá de la hipnosis7.
Inhibe el receptor del N-Metil-D-Aspartato (NMDA) de forma dosis dependiente, resultando en un bloqueo de la actividad sináptica excitatoria, produciendo así efectos anestésicos, analgésicos y sedativos7.
El principal agonista endógeno del receptor NMDA es el glutamato, el neurotransmisor excitador predominante en el SNC. La activación de este canal desempeña un papel fundamental en la cognición, el dolor crónico, la tolerancia a los opiáceos y la regulación del estado de ánimo, y se considera el principal receptor implicado en los fenómenos de sensibilización central y windup. Sin embargo, el antagonismo del receptor NMDA no es el único mecanismo de sus efectos analgésicos y antidepresivos (Fig. 2). En dosis elevadas, la ketamina activa diversos receptores opioides (mu > kappa > sigma) y sobre una multitud de otras vías no NMDA que desempeñan papeles integrales en la regulación del dolor y del estado de ánimo, incluidos los efectos antagonistas sobre los receptores colinérgicos nicotínicos y muscarínicos y el boqueo de canales sodio activados por voltaje, así como activación de los receptores dopaminérgicos, serotoninérgicos, canales de calcio activados por voltaje, facilitación de la señalización del ácido γ-aminobutírico A (GABA-A) y la potenciación de las vías moduladoras descendentes3.
Figura 2. Efectos y lugares de acción de la ketamina (adaptado de Bhargab et al., 2021. Ketamine: more than just NMDA blocker. Research Gate).

Otro sitio de acción recientemente estudiado es el bloqueo de los canales de sodio voltaje dependientes, de manera similar a los anestésicos locales. Se ha demostrado que aumenta la duración del bloqueo en comparación con los anestésicos locales administrados aisladamente, tanto en anestesia neuraxial como en anestesia regional periférica, aunque la escasa calidad de la evidencia hace que sean necesarios más estudios para establecer su papel como coadyuvante de los anestésicos locales8.
La ketamina produce la llamada “anestesia disociativa”: hipnosis con efectos psicomiméticos, analgesia y sedación, con estimulación simpática y mantenimiento de la mecánica ventilatoria7.
A dosis subanestésicas tiene efectos analgésicos similares a los opioides mayores como la morfina o el fentanilo. Debido a sus efectos secundarios y su potencial de abuso, aún no está claro el papel exacto de la ketamina como analgésico, especialmente en el ámbito ambulatorio o comunitario. Sin embargo, cada vez se reconoce más que desempeña un papel importante en la analgesia multimodal7.
Comercializada inicialmente como anestésico, está ganando cada vez más importancia en el tratamiento del dolor agudo perioperatorio y del dolor crónico, tanto oncológico como no oncológico, con vías de administración validadas que incluyen la intravenosa, la intramuscular, la subcutánea, la epidural, la intratecal, la intraarticular, la intranasal, la oral y la tópica9.
Su aplicabilidad como analgésico tiene resultados en pacientes con dolor crónico, sobre todo en síndromes que tienen una etiología predominantemente neuropática (15-25%)10, en los que los fenómenos de sensibilización central son más relevantes3. Las patologías con más evidencia a favor son el dolor regional complejo (siendo esta su indicación más común), el dolor tras lesión medular, dolor crónico neuropático y dolor del miembro fantasma3.
También se han obtenido resultados beneficiosos en pacientes con dolor oncológico de origen no neuropático, dolor isquémico o para manejo de las migrañas, aunque con menor evidencia11.
Recientemente, se ha descubierto que la ketamina puede revertir de manera rápida y significativa la ideación suicida en pacientes con depresión, beneficios que se manifiestan en cuestión de horas y permanecen hasta días después de la administración7. La estrecha relación entre el dolor crónico y la depresión, dos condiciones que en la mayoría de las ocasiones suelen coexistir, potencia el efecto analgésico de la ketamina12.
Otro beneficio a destacar es que aumenta la eficacia de los opioides coadministrados. Al bloquear los receptores NMDA puede prevenir o reduce la tolerancia y la hiperalgesia que producen estos12, pudiendo contribuir así a una disminución en las dosis de opioides utilizadas en tratamientos prolongados.
Asimismo, su aplicabilidad en el contexto de dolor agudo podría considerarse en el periodo perioperatorio, sobre todo en: pacientes con dolor severo refractario, aquellos con tolerancia o dependencia a opioides o, en pacientes con patologías como apnea obstructiva del sueño, en las que es conveniente reducir la dosis de opioides para prevenir la depresión respiratoria11.
Otros efectos que se le pueden atribuir son: broncodilatación en asma refractaria, modulación autoinmune, inhibición tumoral, efecto antinflamatorio (sobre todo en sepsis), neuroprotección y uso en estatus epiléptico refractario3.
El dolor crónico oncológico tiene una etiología multifactorial, lo que hace imprescindible un enfoque multimodal para su evaluación y manejo. Pese a que la ketamina ha ganado interés clínico, es necesario realizar más estudios para evaluar su eficacia y seguridad a largo plazo, estandarizar vías de administración y dosis adecuadas. Aunque no se considere un fármaco de primera línea, debería considerarse como opción potencial en el abordaje multimodal de los síndromes de dolor crónico, especialmente aquellos refractarios al tratamiento estándar.