CASO CLÍNICO
Paciente de 56 años, hipertenso en tratamiento farmacológico, carpintero de profesión. Sufre un accidente con traumatismo en el borde radial de la muñeca derecha con resultado de una herida cutánea y lesión tendinosa con déficit de extensión del pulgar. En un primer tiempo se realiza sutura de la herida y al mes siguiente cirugía de reparación tendinosa. El paciente evoluciona con dolor neuropático espontáneo grave y constante tipo disestésico. A la exploración física se aprecia dolor evocado de tipo hiperalgesia y alodinia mecánica en los territorios de los nervios cutáneo antebraquial lateral (NCAL) y radial superficial (NRS), con signo de Tinel sobre el tronco del NRS y una pérdida de movilidad del dedo pulgar, probablemente limitada por dolor. Una electromiografía confirma la lesión del NRS de tipo axonotmesis parcial grave, con pérdida axonal del 90% respecto al lado contralateral. Se realiza cirugía de resección del neuroma de la rama sensitiva del nervio radial y neurotomía del nervio interóseo posterior. No se aprecian cambios en la intensidad y características del dolor. Se interviene una segunda vez realizándose una resección del neuroma, pero tampoco hay mejoría. Se practica una tercera cirugía realizándose una reconstrucción microquirúrgica con aloinjerto de la rama sensitiva del nervio radial, pero tampoco esta vez el paciente experimenta alivio del dolor. Finalmente se realiza una nueva neurectomía del NRS. En total se practican cuatro cirugías de nervio y ninguna de ellas consigue mejorar la clínica de dolor neuropático grave, que sigue siendo constante y afecta significativamente a la calidad de vida del paciente.
Se deriva al paciente a la Unidad del Dolor. Se realiza tratamiento con anticomiciales, gabapentinoides, tramadol, lidocaína tópica y parches de capsaicina que no son efectivos. Tampoco lo son la radiofrecuencia pulsada del NRS ni la terapia PENS. Llegados a este punto, se plantea la implantación de un neuroestimulador periférico. Estamos ante un paciente con dolor neuropático probable, ya que presenta dolor asociado a signos sensitivos en un área neuroanatómica congruente con la lesión neurológica. Para confirmar el diagnóstico de dolor neuropático periférico, se asocia al estudio electroneurográfico de fibra gruesa mielinizada sensitiva, un estudio sensorial cuantitativo (QST) para evaluar la función de la fibra fina termoalgésica. El examen neurofisiológico muestra ausencia del potencial sensitivo tanto del NRS como del NCAL derechos. El QST determina un área de hiperalgesia mecánica (128 mN) en el territorio cutáneo de los nervios radial superficial y cutáneo antebraquial lateral (Figs. 1 y 2). El Termotest Cuantitativo demuestra, en estos territorios, una hipoestesia al frío con anestesia al calor, umbral de detección del dolor por frío conservado y analgesia al calor, con una hiperalgesia reactiva al calor supraumbral (Fig. 3 y Tabla 1). Una vez confirmado el diagnóstico, con el objetivo de determinar en qué nervio se implantará el electrodo del neuroestimulador se llevan a cabo una serie de bloqueos anestésicos diagnósticos ecoguiados con lidocaína al 2%. En primer lugar se bloquea el NRS proximal a la neurectomía, tras media hora el paciente refiere notar el mismo dolor junto a la hiperalgesia a la exploración. En segundo lugar, se bloquea el NCAL sin éxito. En tercer y último lugar se realiza el bloqueo anestésico del nervio radial proximal al codo antes de la división en las ramas sensitiva y motora. Esta vez el paciente refiere disminución del dolor en un 70%. Se procede a la implantación del neuroestimulador periférico sobre el nervio radial dejando los polos de estimulación en el mismo punto donde se había realizado el bloqueo anestésico. La terapia de neuroestimulación resulta satisfactoria el primer mes y a los 4 meses, el paciente experimenta una mejoría significativa y progresiva del dolor sobre todo en la región del antebrazo y muñeca, no así en el área de la mano y los dedos. No toma ninguna medicación oral, únicamente se aplica parches de lidocaína tópica oca- sionalmente. Actualmente continúa con controles periódicos en la Unidad del Dolor.
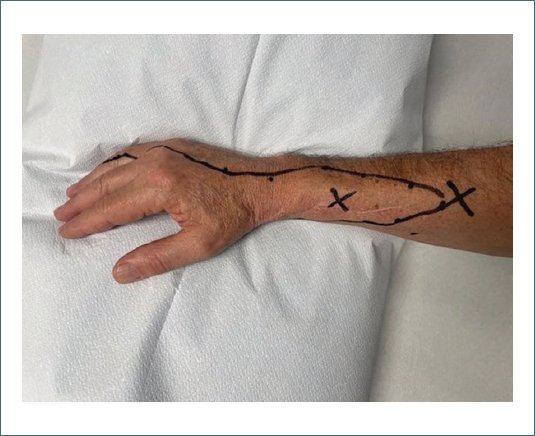
Figura 1. Línea negra: área de hiperalgesia mecánica. Cruces: signos de Tinel.
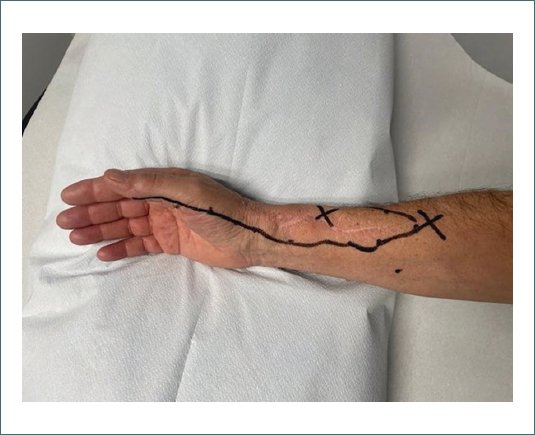
Figura 2. Línea negra: área de hiperalgesia mecánica. Cruces: signos de Tinel.
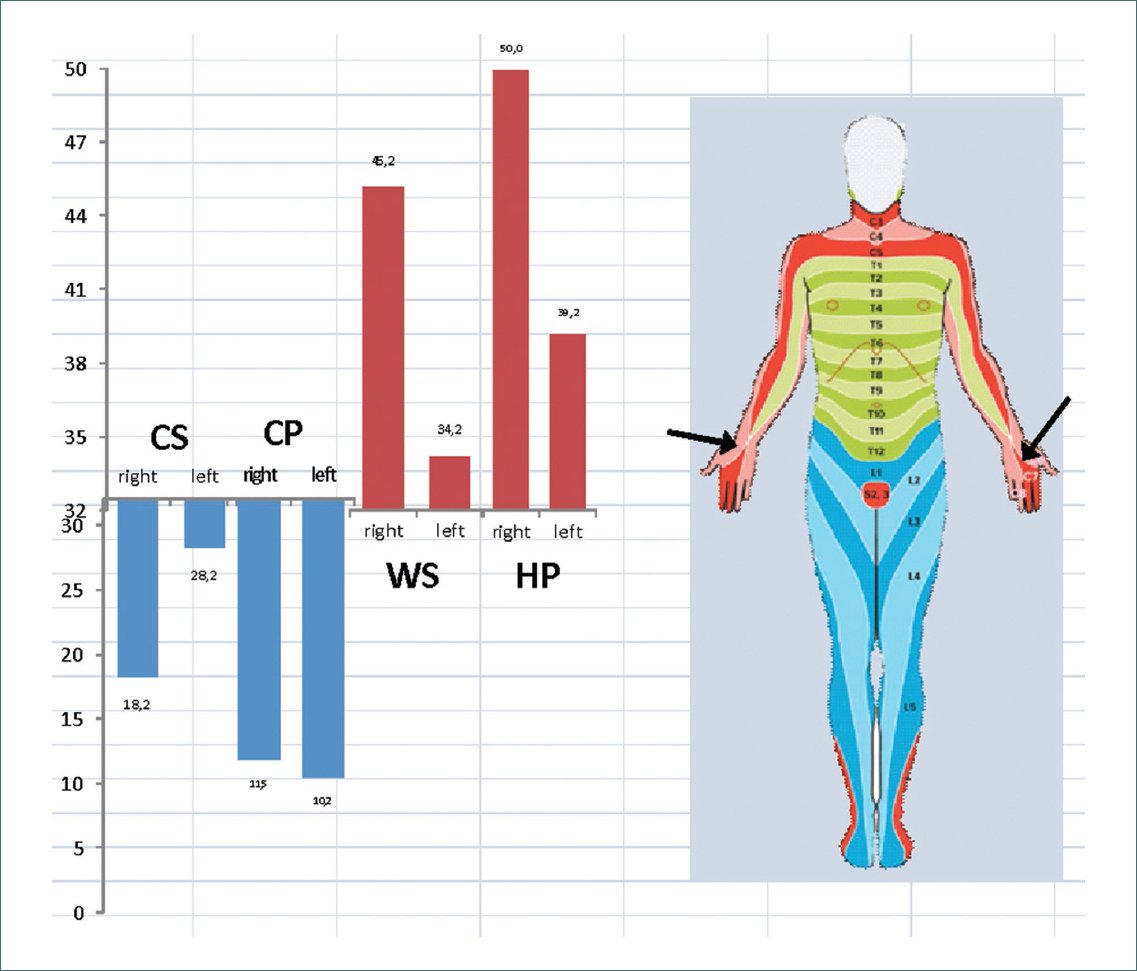
Figura 3. Termotest cuantitativo: barras azules corresponden a la media de umbrales para la sensación de frío (CS) y dolor por frío (CP) en el área a estudio y su comparativa con la misma área en el lado contralateral. Las barras rojas corresponden a sensación de calor (WS) y dolor por calor (HP).
Tabla 1. Método de límites realizado en el área de estudio y comparándolo con la misma área en el lado contralateral, media de 3 repeticiones para el valor umbral de la sensación de frío (CS), sensación de calor (WS), dolor por frío (CP) y dolor por calor (HP)
| CS | WS | CP | HP | |
|---|---|---|---|---|
| Derecha | 18,2 | 45,2 | 11,5 | 50,0 |
| Izquierda | 28,2 | 34,2 | 10,2 | 39,2 |
DISCUSIÓN
Se describe un cuadro clínico caracterizado por dolor neuropático periférico de origen traumático por una lesión del NRS, resistente a múltiples abordajes terapéuticos, cuya evolución a la cronicidad desafía las estrategias terapéuticas habituales y pone de manifiesto las dificultades diagnósticas y terapéuticas asociadas al dolor neuropático periférico. La ausencia de mejoría clínica tras cuatro cirugías y múltiples tratamientos farmacológicos e intervencionistas obliga a replantear el comportamiento neuroplástico del sistema somatosensorial y la importancia de un enfoque en el proceso diagnóstico más preciso.
Este trabajo surge de la experiencia acumulada de casos similares que afectan, en concreto, al NRS. Nos preguntamos si el hecho de que sea un nervio cutáneo, protegido únicamente por tejido celular subcutáneo y piel, tiene relación con la gravedad del dolor causada por lesiones incluso de leve intensidad. Casos similares suceden con lesiones de otros nervios cutáneos e igualmente expuestos, como la rama infrapatelar del nervio safeno, el nervio sural o el nervio peroneo superficial. Todos ellos son fácilmente identificables mediante su palpación en la exploración física.
Uno de los aspectos más desconcertantes de este caso es la persistencia de síntomas dolorosos intensos a pesar de haber realizado la neurectomía del NRS. Este hecho plantea diversas hipótesis. En primer lugar, cabe considerar la existencia de anastomosis preexistentes entre el NRS con otros nervios sensitivos del brazo y antebrazo, como el NCAL1 y el nervio cutáneo antebraquial medial (NCAM). En varios estudios anatómicos se han descrito variantes anatómicas que permiten estas conexiones. La proximidad de estos nervios hace posible la existencia de puentes nerviosos entre ellos. Podrían existir también conexiones entre el NRS y la rama motora del nervio radial. De hecho, al paciente se le practica una neurotomía del nervio interóseo posterior con la intención de mejorar el dolor, pero no hemos encontrado bibliografía que respalde esta teoría.
Hay evidencia de superposición de áreas de inervación cutánea entre el NRS y el NCAL, especialmente en la región del primer espacio interdigital dorsal2–4. Démouline et al., describen en dos disecciones del dorso de la muñeca en cadáver la presencia de inervación con combinación del NRS y el NCAL, evidenciando territorios cutáneos superpuestos con presencia de anastomosis entre estos dos nervios, y en el otro caso, la inervación cutánea provenía únicamente del NCAL2. Se han documentado más casos de suplantación completa del territorio del NRS por el NCAL3. Incluso se ha descrito la inervación completa del dorso de la mano por el NRS en ausencia de la rama sensitiva del cubital o por superposición5. Estas variaciones pueden ser preexistentes o podrían desarrollarse como parte de un proceso de reinervación colateral tras una lesión. La persistencia del dolor tras la neurectomía sugiere la posibilidad de que otras fibras sensoriales vecinas hayan invadido el territorio previamente inervado por el NRS mediante un proceso de “sprouting” (brote axonal), fenómeno bien descrito en estudios sobre plasticidad periférica tras lesiones nerviosas. Este planteamiento se apoya en estudios clásicos y en la evidencia más actual que demuestra reinervación colateral y reorganización de los mapas sensoriales tras una lesión del nervio periférico en un proceso de neuroplasticidad6. Recordemos que después de sufrir el traumatismo, el paciente presenta dolor espontáneo disestésico en el territorio cutáneo de la mano que posiblemente se deba a la presencia de neuromas de amputación. En cambio, tras haber realizado la última neurectomía, el dolor que presenta es dolor evocado en forma de hiperalgesia y alodinia mecánica, que persisten incluso después del bloqueo anestésico del NACL y con el uso del neuroestimulador. Este fenómeno se corresponde con mecanismos más complejos de sensibilización central, posiblemente en relación con la reinervación de fibra nociceptiva que, aunque escasa, se nutra de un circuito de transmisión aberrante amplificado a nivel central7. El QST demuestra presencia de cierta inervación de la fibra termoalgésica en la mano, ya que evidencia respuestas exacerbadas con estímulos supraumbrales, lo que se traduciría en respuesta hiperpáticas vehiculizadas por las escasas fibras nociceptoras “supervivientes”. Es posible que estas fibras surjan de anastomosis del NCAL y logren transmitir los suficientes potenciales de acción, incluso después del bloqueo anestésico, que una vez alcanzados centros superiores como el ganglio de la raíz dorsal, se amplifiquen en forma de sensibilización central. Además, la regeneración anómala de fibras nerviosas puede alterar la distribución anatómica y funcional de canales iónicos de sodio voltaje dependientes, lo que podría contribuir a una menor efectividad de los anestésicos locales en zonas lesionadas.
Creemos que la mejoría del dolor en el antebrazo y la muñeca con el bloqueo anestésico se debe a reinervación por fibras sensitivas procedentes del nervio radial, cuyos potenciales de acción son sensibles a la terapia de neuroestimulación periférica.
En el dolor neuropático existe una gran heterogeneidad de los mecanismos fisiopatológicos, los signos y síntomas somatosensoriales son múltiples y conforman diferentes fenotipos sensoriales según sea su combinación y en ocasiones pueden confundirse con dolor nociceptivo. Estos perfiles sensoriales podrían estar relacionados con los mecanismos subyacentes y no con la enfermedad causante, lo que podría tener implicaciones terapéuticas8. Con el fin de hacer un diagnóstico preciso, y siguiendo las recomendaciones de 2008 por un grupo internacional de expertos en dolor neuropático9, se realizó el estudio sensorial cuantitativo (QST) que fue fundamental para confirmar el diagnóstico y caracterizar el fenotipo sensorial. El paciente muestra un patrón mixto con hipoestesia al frío, anestesia al calor e hiperalgesia supraumbral, lo que indica disfunción de fibras finas y sensibilización nociceptiva.
Es recomendable antes realizar cualquier intervención sobre un nervio, ya sea quirúrgica o no, realizar bloqueo anestésico diagnóstico10. En nuestro caso fueron de gran utilidad a la hora de decidir en qué nervio se iba a implantar el neuroestimulador periférico. La neuroestimulación periférica se ha consolidado como una estrategia eficaz en casos seleccionados de dolor neuropático refractario11.
Este caso ejemplifica la complejidad del dolor neuropático tras lesiones nerviosas y cirugías repetidas. El conocimiento de las posibles variaciones anatómicas, los diferentes mecanismos fisiopatológicos y perfiles sensoriales del dolor neuropático, es esencial para definir el diagnóstico, personalizar el tratamiento y evitar intervenciones ineficaces.
CONCLUSIÓN
El dolor neuropático grave tras lesión de un nervio cutáneo puede estar condicionado por variaciones anatómicas como anastomosis o superposición de áreas sensitivas, que deben tenerse en cuenta ante los fenómenos de brote axonal y neuroplasticidad periférica. Estos mecanismos, junto con la neuroplasticidad central y la diversidad de fenotipos sensoriales, dificultan el diagnóstico de dolor neuropático periférico. Un estudio diagnóstico preciso, mediante pruebas como el QST y los bloqueos anestésicos, permite confirmar el diagnóstico y evitar tratamientos innecesarios y sus posibles efectos adversos.